Негашеная известь формула химическая
Оксид кальция. Свойства и меры предосторожности
Оксид кальция — неорганическое соединение с формулой CaO. В литературе также можно встретить такие его названия, как негашеная известь, окись кальция, жженая известь, кирабит, «кипелка».
Негашеная известь называется так для отличия от гашеной извести, когда при соединении оксида кальция с водой проходит бурная реакция — известь «гасится» водой. Получается гашеная известь Ca(OH)2, востребованная во многих областях.
Жженой известью реактив называют с отсылкой на способ получения: известь (карбонат кальция CaCO3) обжигают до тех пор, пока она не начинает разлагаться, в результате чего получается жженая известь (окись кальция).
Обычно негашеной или жженой известью называют техническую квалификацию реактива.
Получить окись кальция можно разными методами.
• Промышленный способ описан выше: разложением известняка CaCO3 при нагревании.
• Разложением при нагревании гидроокиси кальция или солей кальция (солей определенных кислот, содержащих кислород). Например, разложением нитрита кальция Ca(NO3)2 получают CaO высокой чистоты.
• Прямым окислением (сжиганием) кальция в воздухе.
| Полнолицевая маска «ЗМ» серии 6900 | Кальций окись "ч" | Перчатки "Неотоп" химостойкие (Ansell) (9,5-10) |
Свойства
Реагент представляет собой порошкообразное вещество белого или сероватого цвета без запаха. Структура кристаллов подобна структуре поваренной соли. Реактив гигроскопичен, поглощает из воздуха влагу и углекислый газ. Хорошо растворяется в глицерине, не растворяется в этиловом спирте. В воде не растворяется, а вступает с ней в химическую реакцию. Не горит. Токсичен.
С химической точки зрения очень активное соединение, осно́вный оксид. Реагирует с водой с образованием щелочи Ca(OH)2 и выделением большого количества тепла. В реакции с кислотами и кислотными оксидами образует соли. Взаимодействует с углеродом (получается карбид CaC2). Вступает в реакцию с метиловым спиртом, оксидами металлов, с металлами, с хлором, бромом и другими галогенами, углекислым газом, серой, фосфором, кремнием и многими другими веществами.
Вступает в реакцию с метиловым спиртом, оксидами металлов, с металлами, с хлором, бромом и другими галогенами, углекислым газом, серой, фосфором, кремнием и многими другими веществами.
Меры предосторожности
Негашеная известь — едкое вещество, которое относится ко 2-му (высокоопасному) классу веществ. Особенно опасно смешивать оксид с водой. Во-первых, можно обжечься; во-вторых, образующаяся щелочь разъедает кожу. Но даже без воды оксид действует на кожу как щелочь: вытягивает влагу из кожи, разрушает белки, омыляет жиры, вызывает химический ожог.
Опасность представляют известковая пыль, ее пары и аэрозольные частицы. Они попадают в органы дыхания, вызывая раздражение и кашель. При попадании в легкие могут вызвать пневмонию. Проглатывание оксида кальция вызывает ожог пищевода и желудка.
Очень опасен реактив для слизистых носа и особенно глаз. Способен вызвать язвы слизистой носа и даже прободение носовой перегородки.
Пострадавшему от контакта с химикатом обязательно следует вызвать скорую помощь. До приезда скорой нужно хорошо промыть место поражения: кожу, глаза, пищевод.
До приезда скорой нужно хорошо промыть место поражения: кожу, глаза, пищевод.
При работе с оксидом кальция (как на производствах, так и в быту) следует использовать защитную одежду; респиратор; очки; перчатки, стойкие к щелочам. На предприятиях обязательно контролируют ПДК реактива в воздухе. Рабочее место должно располагаться в помещении с общей принудительной вентиляцией. Места высокого риска пыления дополнительно снабжаются локальной вытяжной вентиляцией.
Хранят реактив в герметичной упаковке (многослойные ламинированные бумажные мешки), на сухих крытых складах с хорошей механической вентиляцией, при комнатной температуре. Реактив несовместим с водой, фтором, сильными кислотами.
В лабораториях работы следует проводить в вытяжном шкафу. Хранят реактив в герметичных стеклянных или пластиковых сосудах с обязательными предупреждающими этикетками.
Оксид кальция – формула, реакции получения, тип химической связи
4.7
Средняя оценка: 4.7
Всего получено оценок: 148.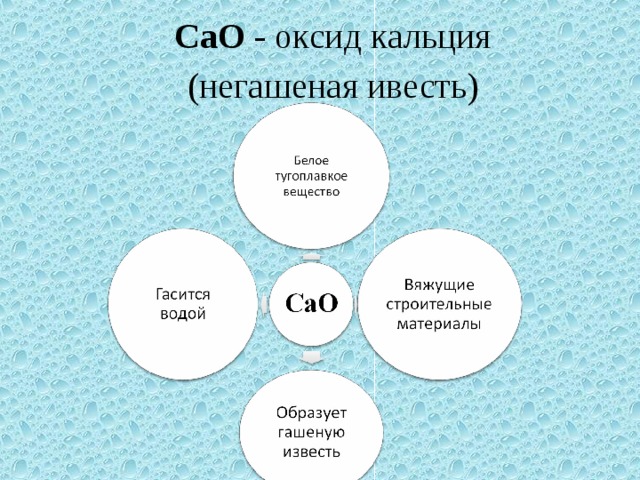
4.7
Средняя оценка: 4.7
Всего получено оценок: 148.
Негашёная известь – это оксид кальция. Его получают в лабораториях и промышленным путём из природных материалов. Вещество активно используется в строительстве и промышленности.
Физические свойства
Оксид кальция – неорганическое кристаллическое вещество в виде белого или серо-белого порошка без запаха и вкуса. Твёрдое вещество кристаллизуется в кубические гранецентрированные кристаллические решётки по типу хлорида натрия (NaCl).
Рис. 1. Кубические гранецентрированные кристаллические решётки.Общее описание вещества представлено в таблице.
| Признак | Значение |
| Формула соединения оксид кальция | CaO |
| Температура плавления | 2627°C |
| Температура кипения | 2850°C |
| Растворимость | В глицерине. |
| Молярная масса | 56,077 г/моль |
| Плотность | 3,37 г/см3 |
| Химическая связь в кристалле | Ионная |
Оксид кальция – едкое вещество, относящееся ко второму классу опасности. Агрессивные свойства проявляет при взаимодействии с водой, образуя гашёную известь.
Рис. 2. Порошок оксида кальция.Получение
Оксид кальция также называют жжёной известью из-за способа получения. Получают негашёную известь путём нагревания и разложения известняка – карбоната кальция (CaCO3).
Это природное вещество, встречающееся в форме минералов – арагонита, ватерита, кальцита. Входит в состав мрамора, мела, известняка.Реакция получения оксида кальция из известняка выглядит следующим образом:
CaCO3 → CaO + CO2.
Кроме того, негашёную известь можно получить двумя способами:
Реакции протекают при высоких температурах. Температура сожжения известняка – 900-1200°C. При 200-300°C на поверхности металла начинает образовываться оксид. Для разложения солей и гидроксида необходима температура в 500-600°C.
Температура сожжения известняка – 900-1200°C. При 200-300°C на поверхности металла начинает образовываться оксид. Для разложения солей и гидроксида необходима температура в 500-600°C.
Химические свойства
Оксид кальция является высшим оксидом и максимально проявляет окислительные свойства. Соединения взаимодействует с неорганическими веществами и свободными галогенами. Основные химические свойства оксида приведены в таблице.
| Реакции | Что образуется | Молекулярное уравнение |
| С водой | Образуется гидроксид (гашёная известь). Реакция протекает бурно с выделением тепла | CaO + H2O → Ca(OH)2 |
| С кислотами | Растворяется, образуя соли | CaO + 2HCl → CaCl2 +H2O |
| С оксидами неметаллов (кислотными остатками) | Образуются соли | CaO + SO2 → CaSO3 |
| С углеродом при нагревании | Образуется карбид кальция | CaO + 3С → СаС2 + CO |
| С алюминием | Восстанавливает кальций. | 3CaO + 2Al → Са + Al2O3 |
Применение
Оксид используется в пищевой промышленности в качестве:
- улучшителя муки и хлеба;
- пищевой добавки Е529;
- регулятора кислотности;
- питательной среды для дрожжей;
- катализатора гидрогенизации (присоединения водорода) жиров.
Кроме того, негашёная известь применяется в химической и строительной промышленности для производства различных веществ:
- масел;
- стеарата кальция;
- солидола;
- огнеупорных материалов;
- гипса;
- высокоглиноземистого цемента;
- силикатного кирпича.
Что мы узнали?
Оксид кальция или негашёная известь – кристаллическое вещество, бурно реагирующее с водой и образующее гашёную известь. Широко используется в промышленности, в частности пищевой и строительной. Зарегистрирован как пищевая добавка Е529. Имеет высокие температуры плавления и кипения, растворяется только в глицерине. Образуется при сжигании карбоната кальция. Проявляет окислительные свойства, образует соли с оксидами и кислотами, взаимодействует с углеродом и алюминием.
Зарегистрирован как пищевая добавка Е529. Имеет высокие температуры плавления и кипения, растворяется только в глицерине. Образуется при сжигании карбоната кальция. Проявляет окислительные свойства, образует соли с оксидами и кислотами, взаимодействует с углеродом и алюминием.
Тест по теме
Доска почёта
Чтобы попасть сюда - пройдите тест.
Владимир Комаров
10/10
Сергей Ефремов
4/10
Оценка доклада
4.7
Средняя оценка: 4.7
Всего получено оценок: 148.
А какая ваша оценка?
Какова формула негашеной извести?(а). $Ca{ \\left( OH \\right) }_{ 2 }$(b). $Ca{Cl}_{2}$(c). СаО(г). $ Ca {so} _ {4}
$
- Подсказка: негашеная известь является основой кальция, не содержащей гидроксильной группы. Негашеная известь реагирует с водой с образованием гидроксида кальция. Это белое кристаллическое твердое вещество, которое доступно в виде белого порошка. 9{ \circ }C }{ \longrightarrow } } Ca{ O }_{ \left( s \right) }+{ { CO }_{ 2 } }_{ \left( g \right) }\uparrow$
Это белое кристаллическое твердое вещество, которое доступно в виде белого порошка. 9{ \circ }C }{ \longrightarrow } } Ca{ O }_{ \left( s \right) }+{ { CO }_{ 2 } }_{ \left( g \right) }\uparrow$
Негашеная известь используется в различных целях, таких как побелка, производство газобетонных блоков, кальций-алюминиевого цемента, стекла, органических химикатов и т. д.
Следовательно, формула негашеной извести - CaO. Значит, вариант в правильный.
Примечание. Не путайте негашеную и гашеную известь. Негашеная известь — это оксид кальция (CaO), а гашеная известь — это гидроксид кальция ( $Ca{ \left( OH \right) }_{ 2 }$ ). Как было показано ранее, гашеная известь образуется при растворении негашеной извести в воде.
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы 12 класса химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал Химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 Химический класс 12 JEE_Main
Какой элемент обладает наибольшим радиусом атомов Химический класс 11 JEE_Main
Фосфин получают из следующей руды А Кальций класса 12 по химии JEE_Main
В Индии по случаю бракосочетания фейерверков класс 12 по химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть отнесены к классу 12 по химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал 12 класса химии JEE_Main
Что из перечисленного является истинным пероксидом A rmSrmOrm2 12 класса химии JEE_Main
Какой элемент обладает наибольшим атомным радиусом А класса 11 химии JEE_Main
Фосфин получают из следующей руды A Химический состав кальция класса 12 JEE_Main
Тенденции сомнения
Британская известковая ассоциация (BLA), часть Ассоциации минеральных продуктов (MPA)
Известковый цикл
Известковый цикл — один из самых известных примеров химии в природе. Этот жизненный цикл происходит как для извести с высоким содержанием кальция, так и для продуктов из доломитовой извести.
Этот жизненный цикл происходит как для извести с высоким содержанием кальция, так и для продуктов из доломитовой извести.
- Когда известняк/мел (карбонат кальция) обжигается в печи, он превращается в негашеную известь (оксид кальция) и выделяет углекислый газ.
- В негашеную/негашеную известь можно добавлять воду для получения гашеной извести (гидроксида кальция).
- В течение срока службы известковых продуктов углекислый газ постепенно повторно поглощается известью из воздуха, что известно как рекарбонизация. Химически это начинает превращать известь обратно в карбонат кальция.
Известняк/мел
- Химическая формула: CaCO 3 (карбонат кальция)
- Молекулярная масса: 100,09
- Разлагается при прокаливании при 900°C с образованием оксида кальция
Кальцинирование (или обжиг)
Обжиг известняка/мела происходит примерно при 1000°C. Реакция для термического разложения карбоната кальция заключается в следующем:
Реакция для термического разложения карбоната кальция заключается в следующем:
Caco 3 + HEAT ↔CAO + CO 2
100G 56G 44G
Эта химическая реакция производит быстрое размер. Различные печи используются для разных видов известняка/мела и для разных видов продукта (подробнее см. «Как производится известь»).
Негашеная известь
- Химическая формула: CaO
- Молекулярная масса: 56,08
- Плавится при 2614°С, кипит при 2850°С
- Гидратация (или гашение)
Основным компонентом негашеной извести является оксид кальция. Его качество часто зависит от ряда определенных факторов, включая физические свойства, реакцию на воду и химический состав. Как наиболее доступная и недорогая щелочь, негашеная известь играет важную роль в широком спектре промышленных процессов.
Гашеная известь
- Химическая формула: Ca(OH) 2
- Молекулярная масса: 74,09
- Разлагается при 580°C с образованием оксида кальция
Добавление воды к негашеной извести вызывает экзотермическую реакцию (выделяет тепло) и гашеную известь.
Реакция гидратации негашеной извести выглядит следующим образом:
CaO + H 2 0 = Ca(OH) 2 + тепло
Установки гидратации относительно сложны и могут питаться избыточными сортами негашеной извести. Гашеная известь, несмотря на свое название, в основном сухая и обычно содержит менее 1% непрореагировавшей воды. По оценкам, от 10% до 15% негашеной извести, производимой в развитых странах, перерабатывается в гашеную известь (процент, который, вероятно, выше для стран, не имеющих крупной сталелитейной промышленности). Гашение извести включает производство дисперсии гидроксида кальция в воде с получением продукта, известного как известковое молоко или известковая замазка.
Рекарбонизация
Процесс рекарбонизации по существу противоположен процессу прокаливания/обжига. И негашеная, и гашеная известь при длительном воздействии воздуха начинают втягивать углекислый газ из атмосферы. Таким образом, это заменяет оксидный компонент химического вещества и возвращает известь примерно в исходное состояние – известняк или мел.
 В этаноле не растворяется, с водой образует гидроксид
В этаноле не растворяется, с водой образует гидроксид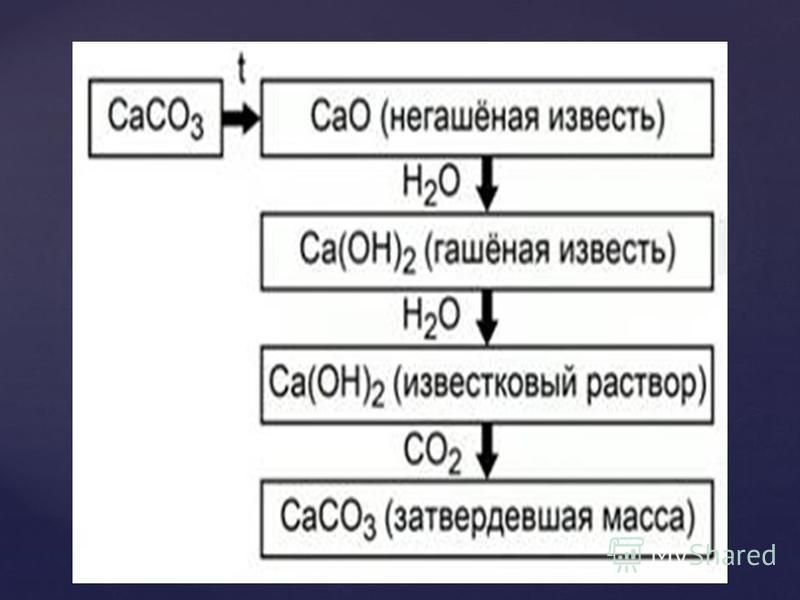 Образуется оксид алюминия
Образуется оксид алюминия